Патина и ее виды
Патина – это защитная пленка, которая покрывает медь при окислении на воздухе. Она необходима для предохранения изделий от дальнейшего разрушения. Патина может делиться по нескольким категориям:
 Патина может проявляться различными оттенками естественным путем
Патина может проявляться различными оттенками естественным путем
- благородная;
- «дикая».
Благородная патина на медных предметах имеет черный цвет. Она защищает его от дальнейшего окисления и разрушения поверхности.
«Дикая» патина имеет зеленый налет. Она появляется на изделиях во влажной среде. Почему же она не ценится? Потому что, такой ее вид является следствием неправильного ухода за металлом, вследствие чего на нем появляются углубления, которые являются коррозией.
Проявляется она в образовании на металле каверз, то есть, многочисленных углублений. Дикую патину с поверхности изделий можно убрать только механической чисткой. Это может испортить внешний вид, так как зеленый налет будет снят вместе с его верхним слоем металла.
 Искусственное патинирование для придания медным изделиям декоративного вида
Искусственное патинирование для придания медным изделиям декоративного вида
Также патина делится на 2 вида:
- естественную;
- искусственную.
Естественная патина появляется на поверхности изделиях со временем. И именно она считается самой ценной. Для ее появления требуется немного времени. Тонкая пленка будет видна уже через год. Хороший толстый слой появляется только за 80–100 лет. Все зависит от погодных условий, климата страны и состава атмосферы.
Искусственная патина сейчас особенно популярна. Ее цвет делают близким не только к благородному черному, но и к зеленому. Такой процесс называется патинированием. На бронзе она получается лучше, чем на латуни.
Но почему же искусственное патинирование применяется не везде? Для придания современным предметам интерьера из меди ее стараются не использовать. Потому что основа искусственной патины — это лаки, воски и краски, которые изолируют метал, и мешают ему покрываться ценным естественным налетом.
Воздействие водной среды
В воде скорость коррозии меди зависит от наличия в ее составе оксидных пленок и растворенного кислорода. Чаще всего металл подвергается ударной или точечной коррозии. Чем насыщеннее вода кислородом, тем быстрее протекают процессы коррозии меди. Пагубно влияют воды, содержащие ионы хлора и низкий уровень pH. Но в целом этот металл оказывает высокое сопротивление водной среде, а разрушению препятствует появление слоя оксида. Так называемая зеленая или черная корка плотно соприкасается с поверхностью изделия и не позволяет разрушающим веществам проникать в металл. Оксид начинает образовываться после двух месяцев непрерывного нахождения изделия в воде. Оксидный слой бывает двух видов:
- карбонат – имеет зеленый цвет и считается более прочным;
- сульфат – имеет темный цвет и рыхлую структуру.
Медь является наиболее предпочтительным металлом для изготовления трубопроводов. Но если, вода, проходящая по медным трубам, в дальнейшем контактирует с алюминием, железом или цинком, то она в значительной мере ускорит коррозию этих металлов. Для предотвращения этого и защиты меди от коррозии используют лужение металла, которое получают путём нанесения на поверхность изделия расплавленного олова. Луженое изделие отличается высокой коррозийной стойкостью, оно не подвержено перепадам температур и способно противостоять негативным атмосферным факторам.
Может ли нержавейка ржаветь?
Существует три группы нержавеющих сталей, каждая из которых имеет свои особенности и специфику применения:
- Коррозионностойкая сталь. Имеет высокую стойкость к коррозии в неосложненных условиях – в быту, на производстве.
- Жаростойкая сталь. Обладает термостойкостью, не ржавеет при повышенных температурах, может применяться на химических заводах.
- Жаропрочная сталь. Остается механически прочной при высоких температурах.

Таким образом, не все виды нержавейки предназначены для эксплуатации в той или иной агрессивной среде. К примеру, использование обычной нержавеющей стали на пищевом производстве, частое мытье с хлорсодержащими средствами вызовет быструю порчу материала. Аналогично применение металла в морской воде приведет к повышению скорости коррозии в разы.
Также ржавчина часто появляется на нержавейке после сварки (термической обработки), которая была произведена без соблюдения определенных правил. После механического повреждения металла последствия будут аналогичными: в месте дефекта возникнет точечная коррозия. Гладкий, полированный материал обычно ржавеет менее интенсивно, чем шероховатый: на последнем элементы коррозии могут появиться гораздо быстрее.
Защита от ржавчины нарушается там, куда попала раскаленная окалина, поскольку от сильного повышения температуры в нежаростойкой стали происходит выгорание легирующих веществ (в основном хрома). После прогорания дыр их края и прилегающие зоны становятся подверженными коррозии, хотя более глубокие слои металла чаще всего остаются неповрежденными. Спасти нержавейку поможет обработка травильными пастами, специальными эмульсиями.
Прочие причины коррозии нержавеющей стали:
- контакт материала с обычной углеродистой сталью (в том числе посредством инструментов, которыми раньше резали простую сталь),
- регулярная чистка металлическими щетками,
- игнорирование механической или химической обработки сварного шва.

Причиной коррозии металла может стать и его изначально низкое качество. Стойкость стали к ржавлению обусловлена присутствием хрома в достаточном количестве. Этот элемент после воздействия воды, воздуха, кислот и щелочей формирует тончайший непроницаемый слой, который не дает материалу ржаветь. Если хрома в составе мало либо он распределен неравномерно, создание и поддержание оксидного слоя становится невозможным.
Подробности
Коррозионные качества
Медь представляет собой металл с высокими свойствами пластичности, которые имеют красновато-золотистый цвет, а после снятия оксидной пленки немного розоватым. По электрической проводимости он будет уступать только серебру, еще характеризуется огромной степенью тепловой проводимости. За счет низкого удельного сопротивления медь используется в электротехнике – она идет на изготовление пластинок из меди, обмотки электрической двигателей, проволоки.
Обратите внимание, что из-за прекрасных антикоррозионных свойств металл будет включаться в сплавы для усовершенствования их инженерных характеристик (латунь, бронза и прочие). В гальванической среде медь превращается в катод, и начинает вступать в электрохимические процессы, а еще вызывает ускоренный процесс ржавления остальных металлов
Медь является неактивным химическим элементов, и потому она практически не взаимодействует с водой (морской или пресной), воздухом. Если воздух сухой, на поверхность материала будет формироваться оксидная пленка с толщиной до 50 мн. Изделие из меди начинает темнеть, становится зеленоватым или коричневым, и это называется патиной. Во множестве случаев патина воспринимается, как покрытие декоративного типа. Коррозионная интенсивность мала при контактировании с разведенной соляной кислотой, но при реакции со множеством остальных кислот, с галогенами, «царской водкой» металл будет окислен с образованием медного карбоната.
Условия для разрушения меди
Воздействие воды
 Защита меди от коррозии очень важна. Скорость ржавления меди в воде будет сильно зависеть от наличия пленки оксидного типа на ее поверхности, а также от уровня насыщенности воды посредством кислорода. Чем больше кислорода в воде, тем интенсивнее будет протекать разрушение материала. В целом же, медь можно считать устойчивой к вредоносному воздействию пресной и соленой воды, и негативно воздействуют на нее лишь растворенные хлорные ионы, а еще низкая степень рН. Прочность, а также неподверженность ржавлению дает возможность применять материалы для изготовления трубопровода.
Защита меди от коррозии очень важна. Скорость ржавления меди в воде будет сильно зависеть от наличия пленки оксидного типа на ее поверхности, а также от уровня насыщенности воды посредством кислорода. Чем больше кислорода в воде, тем интенсивнее будет протекать разрушение материала. В целом же, медь можно считать устойчивой к вредоносному воздействию пресной и соленой воды, и негативно воздействуют на нее лишь растворенные хлорные ионы, а еще низкая степень рН. Прочность, а также неподверженность ржавлению дает возможность применять материалы для изготовления трубопровода.
Обратите внимание, что, если на поверхности изделия, которое покрыто посредством меди, имеет зеленая или даже коричневая оксидная корочка, разрушающие компоненты в малой степени будут проникать внутрь. Как правило, слой оксида образуется спустя 2 месяца нахождения металла в воде
Намного прочнее будет считаться зеленая корочка (то есть карбонатная), рыхлой и не такой крепкой – черная (сульфатная).
В воде из моря степень коррозии почти такой же, как и в обычной, то есть пресной. Лишь при ускорении передвижения воды ржавление станет ударным, и потому более интенсивным. Медь является материалом, который не может обрастать морскими микроскопическими организмами, потому что его ионы губительные для водорослей и моллюсков. Такое свойство металла применяется в судоходстве, а также в рыбном хозяйстве.
Влияние щелочей и кислот
В щелочах медь не будет портиться, потому что материал сам по себе является щелочным, зато кислоты для нее будут являться самыми негативными по воздействию. Самая быстрая и значимая коррозия будет происходить при контактировании с серой и ее кислотными типами соединений, а азотная кислота способна полностью разрушать структуру материала. В концентрированной кислоте медь начинает растворяться, и потому при изготовлении оборудования для промышленности нефтегазового типа требуется дополнительная защита.
Рассмотрим еще кое-что, касающееся коррозии
В почве проживает большое количество микроскопических организмов, которые способны вырабатывать сероводород, так как среда тут кислая, а скорость коррозии меди возрастет. Чем больше отклонение значения рН в стороне окисления, тем скорее будут протекать разрушительные процессы. Если почва оснащена кислородом, то металл начинает окисляться, но ржаветь будет меньше. При длительном нахождении изделий из меди в земле они начинают зеленеть, становятся рыхлыми и способны даже рассыпаться. Краткосрочное пребывание в грунте вызывает образование патины, от которой предмет можно очищать. Кстати, влажный воздух способен плохо сказываться на состоянии материала лишь при длительном контакте, а для начала тоже вызывает образование патины (оксидного слоя). Исключение будет составлять пар, который насыщенный сульфидами, хлоридами, углекислотой – в нем коррозия будет развиваться стремительнее.
Чистка изделий из меди в домашних условиях
Постоянно использующиеся медные изделия чистить нужно регулярно. Подходит простое промывание под краном в моющем средстве для посуды. Вместо этого можно протирать медные предметы санитарным гелем. Если эти способы не приносят чистоты и значительная часть изделия остается покрытой налетом, применяют более агрессивные способы чистки.
Уксус с солью
В этом случае предмет натирают мягкой ветошью с использованием специального средства. Его смешивают из 1 стакана обычного уксуса и 1 ст. л. соли. После очищения предметов от окиси их промывают чистой водой и тщательно протирают.
Другой метод, как почистить медь в домашних условиях, заключается в том, что вещь вываривают в средстве из соли и уксуса. Для него на 3 стакана воды добавляют 1 стакан обычного уксуса и 1 ст. л. пищевой соли. Медное изделие кладут в приготовленный раствор и ставят нагреваться. После 15 минут кипения удается убрать весь зеленый налет. Потом вещь вынимают и промывают под струей воды с моющим средством.
Важно!
Такой способ чистки используют для предметов из меди с защитным покрытием или без него.
Чистка кетчупом
Это легкий и доступный метод почистить медные изделия от налета. В этом случае соусом покрывают поверхность вещи из меди и откладывают на 30 минут. Затем мягкой тряпочкой полируют поверхность, а остатки кетчупа отмывают теплой водой. Этот метод возвращает предмету утерянный блеск. Таким же способом можно очистить медную посуду от патины при помощи кефира.
Чистка солью и лимоном
Таким способом можно почистить медный таз в домашних условиях или крупные изделия из меди до блеска, например, самовары, кастрюли. Лимон разрезают на две части и посыпают место среза крупной поваренной солю. Затем полируют поверхность кухонной утвари.
Можно сделать специальную пасту для чистки меди. Для нее смешивают в одинаковом объеме поваренную соль, пищевую соду и муку, затем добавляют лимонный сок, чтобы образовалась пастообразная масса. Этим средством натирают поверхностный слой предмета до блеска. После очищения вещь отмывают подогретой водой. В итоге медное изделие приобретает зеркальный блеск.

Использование пищевой соды
Удобно применять пищевую соду, чтобы чистить медь в домашних условиях, в сочетании с лимонным соком. Полученной жидкостью протирают поверхностный слой вещи мягкой тряпкой, а затем промывают. Вместо сока лимона можно выполнить чистку меди лимонной кислотой, растворенной в воде и содой.
Другой способ применения пищевой соды для очистки меди от окислов — это кипячение:
- В 1 л воды разводят 1 ст. л. соды и опускают в жидкость изделие полностью.
- Емкость ставят нагреваться и кипятят полчаса, после чего нагрев следует отключить.
- Затем изделие отмывают подогретой водой и полностью вытирают.
Важно!
С помощью предложенного способа убирают зелены налет с медного изделия. Его также используют, чтобы удалить поврежденное лаковое покрытие на медной вещи.
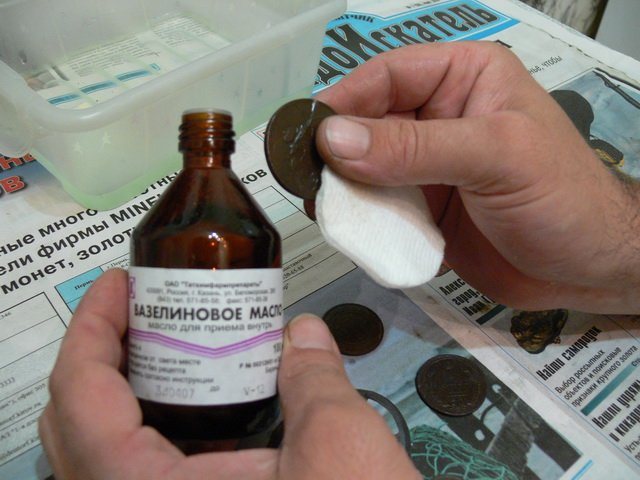
Растительное масло
Прекрасным средством для чистки меди является растительное масло. Еще лучше использовать оливковое. Такой метод хорош своей натуральностью, экологичностью и безвредностью. Поэтому его особенно рекомендуется использовать, когда нужно почистить от окисления ценные вещи.
Для этого масло оливы наливают в глубокую емкость и опускают в него медные предметы. Через 10 дней их вынимают и очищают мягкой щеткой или тряпкой. Затем возвращают на место. Такие действия повторяют каждые 10 дней в течение двух месяцев.
Правильное хранение и эксплуатация медных изделий
Для обеспечения длительного срока службы и сохранения эстетического вида медных изделий необходимо соблюдать определенные правила и рекомендации по их хранению и эксплуатации.
Хранение медных изделий
- Медные изделия следует хранить в специально предназначенных футлярах или мягких тканевых сумках. Это поможет предотвратить повреждения поверхности изделий при хранении и транспортировке.
- Обязательно избегайте воздействия влаги на медные изделия. При хранении следует исключить контакт с водой, особенно если изделие имеет элементы из дерева или других материалов, которые могут поглощать влагу.
- Следует избегать хранения медных изделий рядом с предметами из резины, пластика или латекса, так как они могут вызывать коррозию поверхности меди.
- Рекомендуется хранить медные изделия в прохладном, сухом и хорошо вентилируемом месте, защищенном от прямых солнечных лучей.
Эксплуатация медных изделий
- Перед использованием медных изделий рекомендуется протереть их мягкой тканью или специальным средством для очистки меди. Это поможет удалить пыль, грязь и отложения, которые могут быть причиной коррозии.
- Избегайте длительного контакта медных изделий с кислотными и щелочными веществами, а также с химическими растворами. Это может повредить поверхность меди и вызвать ее коррозию.
- Регулярно очищайте медные изделия от пыли и грязи с помощью мягкой щетки или ткани. В этом случае не рекомендуется использовать жесткие щетки или абразивные материалы, чтобы не поцарапать поверхность меди.
- При использовании медных посуды следует избегать длительного воздействия пламени открытого огня на ее поверхность. Это может вызвать покрытие изделия темными пятнами и изменить его внешний вид.
Следуя этим советам и рекомендациям, вы сможете поддерживать в идеальном состоянии медные изделия, сохранить их эстетическую привлекательность и продлить их срок службы.
Виды коррозии
Как уже говорилось, критериев классификация коррозионных процессов существует множество. Так, различают коррозию по виду распространения (сплошная, местная), по типу коррозионной среды (газовая, атмосферная, жидкостная, почвенная), по характеру механических воздействий (коррозионное растрескивание, явление Фреттинга, кавитационная коррозия) и так далее.
Но основным способом классификации коррозии, позволяющим наиболее полно объяснить все тонкости этого процесса, является классификация по механизму протекания.
По этому критерию различают два вида коррозии:
- химическую
- электрохимическую
Химическая коррозия
Химическая коррозия отличается от электрохимической тем, что протекает в средах, не проводящих электрический ток. Поэтому при такой коррозии разрушение металла не сопровождается возникновением электрического тока в системе. Это обычное окислительно-восстановительное взаимодействие металла с окружающей средой.
Наиболее типичным примером химической коррозии является газовая коррозия. Газовую коррозию еще называют высокотемпературной, поскольку обычно она протекает при повышенных температурах, когда возможность конденсации влаги на поверхности металла полностью исключена. К такому виду коррозии можно отнести, например, коррозию элементов электронагревателей или сопел ракетных двигателей.
Скорость химической коррозии зависит от температуры — при ее повышении коррозия ускоряется. Из-за этого, например, в процессе производства металлического проката, во все стороны от раскаленной массы разлетаются огненные брызги. Это с поверхности металла скалываются частички окалины.
Окалина — типичный продукт химической коррозии, — оксид, возникающий в результате взаимодействия раскаленного металла с кислородом воздуха.
Помимо кислорода и другие газы могут обладать сильными агрессивными свойствами по отношению к металлам. К таким газам относятся диоксид серы, фтор, хлор, сероводород. Так, например, алюминий и его сплавы, а также стали с высоким содержанием хрома (нержавеющие стали) устойчивы в атмосфере, которая содержит в качестве основного агрессивного агента кислород. Но картина кардинально меняется, если в атмосфере присутствует хлор.
В документации к некоторым антикоррозионным препаратам химическую коррозию иногда называют «сухой», а электрохимическую — «мокрой». Однако химическая коррозия может протекать и в жидкостях. Только в отличие от электрохимической коррозии эти жидкости — неэлектролиты (т.е. не проводящие электрический ток, например спирт, бензол, бензин, керосин).
Примером такой коррозии является коррозия железных деталей двигателя автомобиля. Присутствующая в бензине в качестве примесей сера взаимодействует с поверхностью детали, образуя сульфид железа. Сульфид железа очень хрупок и легко отслаивается, освобождая свежую поверхность для дальнейшего взаимодействия с серой. И так, слой за слоем, деталь постепенно разрушается.
Электрохимическая коррозия
Если химическая коррозия представляет собой не что иное, как простое окисление металла, то электрохимическая — это разрушение за счет гальванических процессов.
В отличие от химической, электрохимическая коррозия протекает в средах с хорошей электропроводностью и сопровождается возникновением тока. Для «запуска» электрохимической коррозии необходимы два условия: гальваническая пара и электролит.
В роли электролита выступает влага на поверхности металла (конденсат, дождевая вода и т.д.). Что такое гальваническая пара? Чтобы понять это, вернемся к ряду активности металлов.
Смотрим. Cлева расположены более активные металлы, справа — менее активные.
Если в контакт вступают два металла с различной активностью, они образуют гальваническую пару, и в присутствии электролита между ними возникает поток электронов, перетекающих от анодных участков к катодным. При этом более активный металл, являющийся анодом гальванопары, начинает корродировать, в то время как менее активный коррозии не подвергается.
Схема гальванического элемента
Для наглядности рассмотрим несколько простых примеров.
Допустим, стальной болт закреплен медной гайкой. Что будет корродировать, железо или медь? Смотрим в ряд активности. Железо более активно (стоит левее), а значит именно оно будет разрушаться в месте соединения.
Стальной болт — медная гайка (корродирует сталь)
А если гайка алюминиевая? Снова смотрим в ряд активности. Здесь картина меняется: уже алюминий (Al), как более активный металл, будет терять электроны и разрушаться.
Таким образом, контакт более активного «левого» металла с менее активным «правым» усиливает коррозию первого.
Коррозия металла и способы защиты от нее
Ученые и инженеры разработали множество способов защиты металлических конструкций от коррозии.
Промышленные
Промышленные методы защиты металлических изделий подразделяются на ряд направлений:
- Пассивация. При выплавке стали в ее состав добавляют легирующие присадки, такие, как Cr, Mo, Nb, Ni. Они способствуют образованию на поверхности детали прочной и химически стойкой пленки окислов, препятствующей доступу агрессивных газов и жидкостей к железу.
- Защитное металлическое покрытие. На поверхность изделия наносят тонкий слой другого металлического элемента — Zn , Al, Co и др. Этот слой защищает железо о т ржавления.
- Электрозащита. Рядом с защищаемой деталью размещают пластины из другого металлического элемента или сплава, так называемые аноды. Токи в электролите текут через эти пластины, а не через деталь. Так защищают подводные детали морского транспорта и буровых платформ.
- Ингибиторы. Специальные вещества, замедляющие или вовсе останавливающие химические реакции.
- Защитное лакокрасочное покрытие.
- Термообработка.

Порошковая покраска для защиты от коррозии
Способы защиты от коррозии, используемые в индустрии, весьма разнообразны. Выбор конкретного метода борьбы с коррозией зависит от условий эксплуатации защищаемой конструкции.
Бытовые
Бытовые методы защиты металлов от коррозии сводятся, как правило, к нанесению защитных лакокрасочных покрытий. Состав их может быть самый разнообразный, включая:
- силиконовые смолы;
- полимерные материалы;
- ингибиторы;
- мелкие металлические опилки.
Отдельной группой стоят преобразователи ржавчины — составы, которые наносят на уже затронутые коррозией конструкции. Они восстанавливают железо из окислов и предотвращают повторную коррозию. Преобразователи делятся на следующие виды:
- Грунты. Наносятся на зачищенную поверхность, обладают высокой адгезией. Содержат в своем составе ингибирующие вещества, позволяют экономить финишную краску.
- Стабилизаторы. Преобразуют оксиды железа в другие вещества.
- Преобразователи оксидов железа в соли.
- Масла и смолы, обволакивающие частички ржавчины и нейтрализующие ее.

При выборе грунта и краски лучше брать их от одного производителя. Так вы избежите проблем совместимости лакокрасочных материалов.
Условия разрушения материала
Несмотря на устойчивость к порче, даже медные изделия при определенных условиях могут ржаветь. Меньше всего подобные явления выражены во влажном воздухе, воде, почве, больше – в кислой среде.
Серьезно снизить коррозию можно путем лужения – покрытия меди слоем олова. Качественное лужение дает надежную защиту от повреждений, повышает коррозионную стойкость, делает материал не подверженным действию высоких температур, дождя, града, снега. Срок службы луженых изделий составляет более 100 лет без потери первоначальных свойств.

Влияние воды
Скорость коррозии меди в воде сильно зависит от наличия оксидной пленки на ее поверхности, а также от степени насыщенности воды кислородом. Чем больше содержание последнего, тем интенсивнее протекает разрушение материала. В целом, медь считается стойкой к вредному воздействию соленой и пресной воды, и пагубно влияют на нее только растворенные ионы хлора, низкий уровень pH. Прочность, неподверженность ржавлению позволяет применять материал для изготовления трубопроводов.
Если на поверхности изделия, покрытого медью, имеется коричневая или зеленая оксидная корка, разрушающие вещества в малой степени проникают внутрь. Обычно оксидный слой формируется спустя 60 дней нахождения металла в воде. Более прочной считается зеленая корка (карбонатная), рыхлой и менее крепкой – черная (сульфатная).
В морской воде уровень коррозии практически такой же, как и в пресной. Лишь при ускорении движения жидкости коррозия становится ударной, поэтому – более интенсивной. Медь – материал, который не способен обрастать морскими микроорганизмами, ведь его ионы губительны для моллюсков, водорослей. Это свойство металла используется в судоходстве, рыбном хозяйстве.

Воздействие кислот и щелочей
В щелочах медь не портится, ведь материал сам по себе является щелочным, зато кислоты для нее являются самыми пагубными по воздействию. Наиболее значимая и быстрая коррозия происходит при контакте с серой и ее кислотными соединениями, а азотная кислота и вовсе полностью разрушает структуру материала.
В концентрированных кислотах медь растворяется, поэтому при изготовлении оборудования для нефтегазовой промышленности требует дополнительной защиты. С этой целью применяются ингибиторы – замедлители химических реакций:
- Экранирующие – формируют пленку, которая не позволяет кислотам достигать медной поверхности.
- Окислительные – превращают верхний слой в окись, которая будет вступать в реакцию с кислотами без вреда для самого металла.
- Катодные – увеличивают перенапряжение катодов, чем замедляют реакцию.
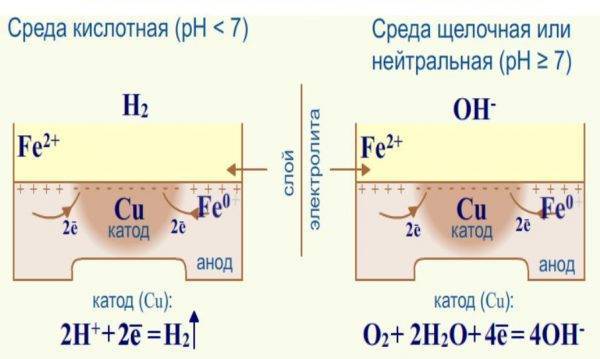
Коррозия в почве и влажном воздухе
В почве проживает множество микроорганизмов, которые вырабатывают сероводород, поэтому среда тут кислая, скорость коррозии меди возрастает. Чем более отклонено значение pH в сторону закисления, тем быстрее протекают процессы разрушения. Если грунт насыщен кислородом, металл окисляется, но ржавеет меньше. При длительном нахождении медных изделий в земле они зеленеют, становятся рыхлыми и могут даже рассыпаться. Краткосрочное пребывание в почве вызывает появление патины, от которой предмет можно очистить.
Влажный воздух плохо сказывается на состоянии материала только при долгом контакте, а вначале тоже вызывает появление патины (оксидного слоя). Исключение составляет пар, насыщенный хлоридами, сульфидами, углекислотой – в нем коррозия развивается стремительнее.
Электрическая защита
Принцип работы электрической защиты основан на использовании анодов и катодов. Аноды, выполненные из материалов с более высокой электрохимической активностью, устанавливаются на медные изделия. Катоды, сделанные из материалов с более низкой активностью, такие как алюминий или цинк, устанавливаются рядом с медью. В результате этого создается гальваническая пара, которая предотвращает окисление меди и коррозию.
Для установки электрической защиты требуются специальные устройства, например, анодные защитные покрытия или гальванические элементы. Они могут быть интегрированы непосредственно в медные изделия или установлены около них. Электрическая защита может быть применена для различных типов медных изделий, включая трубы, кабели, провода и детали.
| Преимущества электрической защиты: | Недостатки электрической защиты: |
|---|---|
| – Эффективность в предотвращении коррозии медных изделий; | – Высокие затраты на установку и обслуживание; |
| – Долговечность защитного покрытия; | – Необходимость использования специальных устройств; |
| – Возможность применения для различных типов медных изделий; | – Требуется постоянное поддержание электрического потенциала; |
Перед установкой электрической защиты необходимо провести тщательное обследование медных изделий и определить их потенциальные уязвимые места. После установки защиты рекомендуется регулярный мониторинг ее работы и проведение профилактических мероприятий.
В целом, электрическая защита является эффективным методом сохранения медных изделий и может быть использована в различных условиях и ситуациях.
Масляная пропитка: эффективный способ сохранить медь без коррозии
Масляная пропитка является давно известным и проверенным способом защиты меди от коррозии. Процесс масляной пропитки заключается в нанесении тонкого слоя масла на поверхность меди. Масло создает защитную пленку, которая предотвращает проникновение воздуха и влаги на поверхность металла и, таким образом, предотвращает образование коррозии.
| Преимущества масляной пропитки: |
|---|
| 1. Защита от окисления: масляная пропитка создает преграду между воздухом и поверхностью меди, не позволяя ей окисляться и образовывать пятна коррозии. |
| 2. Устойчивость к влажности: масляная пленка отталкивает воду, предотвращая проникновение влаги на поверхность меди и, таким образом, защищает металл от коррозии, вызванной влажностью. |
| 3. Простота применения: процесс масляной пропитки не требует особых навыков или специальных инструментов. Достаточно нанести небольшое количество масла на мягкую ткань и протереть поверхность меди до образования равномерного слоя масла. |
| 4. Долговечность: масляная пленка не смывается водой или другими жидкостями, поэтому эффект защиты сохраняется в течение длительного времени. |
Если вы хотите сохранить медные изделия, такие как посуда, лампы или украшения, в идеальном состоянии и предотвратить образование коррозии, рекомендуется регулярно использовать масляную пропитку. Этот простой и доступный способ защитит вашу медь от нежелательных изменений и продлит ее срок службы.
Итак, масляная пропитка является эффективным способом сохранить медь без коррозии. Она предоставляет защиту от окисления, устойчивость к влажности, простоту применения и долговечность. Не забывайте регулярно проводить масляную пропитку медных изделий, чтобы сохранить их в идеальном состоянии на протяжении длительного времени.